Les alcanes




Fin de la page
Suite du cours: Les alcènes
Retour au portail des sciences

Retour au portail de chimie







Etat naturel
Les alcanes ont une grande importance économique.
On les trouve dans les gisements de:
•
•
gaz naturel: surtout du méthane (CH4).
pétrole: mélange très complexe d’hydrocarbures ( C1 à environ C40 ).
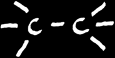
Les liaisons entre carbone sont simples: on parle de liaison σ (sigma , la lettre s en grec). Le carbone se trouve dans l’état d’hybridation sp3.
Exemple:
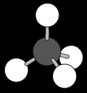
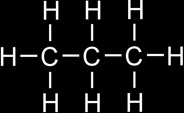
le propane est formé de 3 atomes de C et de [ (2x3) +2 ] atomes de H.
Sa formule brute est C3H8. Sa formule développée s’écrit:
Ce qui veut dire qu’un alcane contient «n» atomes de carbone et «2n+2» atomes d’hydrogène.
les alcanes, autrefois appelés paraffines, sont des hydrocarbures saturés. Leur formule générale est:
Nomenclature
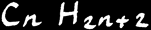
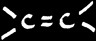

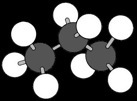
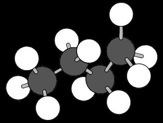
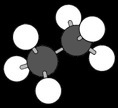
On peut représenter un alcane de différentes manière: avec une formule brute, une formule développée (en 2 dimensions) ou une représentation en 3D. Voyons quelques exemples:
Nom
Formule brute
CnH2n+2
Formule développée 2D
Représentation
3D
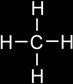
CH4
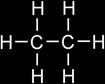
C2H6
Méthane
Ethane
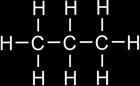
Propane
Butane
C3H8
C4H10
On peut ainsi développer ainsi des chaînes très longues. Plus la molécule est longue et plus sa température d’ébullition est élevée.
Comment s’appelle cet alcane?


Préparation
1.
2.
A partir du pétrole brut: on peut obtenir des alcanes par distillation.
A partir d’hydrocarbures insaturés, par hydrogénation.
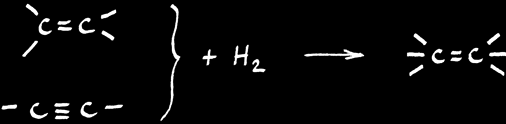
3.
A partir de dérivés halogénés (halogénures d’alkyles).


Exemple:
4.
A partir de fonctions oxygénées.


Réactivité
Les alcanes (parfois appelés paraffines, «sans affinité») sont peu réactifs: ils ne possèdent que des électrons sigma peu disponibles. Ils sont par conséquent très stables.
Seules les réactions de substitution son possibles: il n’y a pas d’additions contrairement aux alcènes et alcynes).
Les liaisons entre C-H et C-C sont covalentes. Elles sont peu ou pas polarisées.
•
•
•
1.
2.
3.
Combustion:
Halogénation:
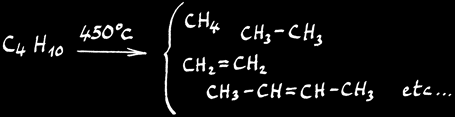
Pyrolyse et isomérisation:



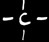
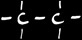
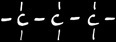
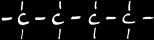
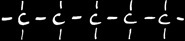
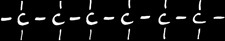
nombre
d'atomes de C
préfixe
Exemple
1
2
3
4
5
6
....
méth...
éth...
prop...
but...
pent...
hex...
méthane
éthane
propane
butane
pentane
hexane
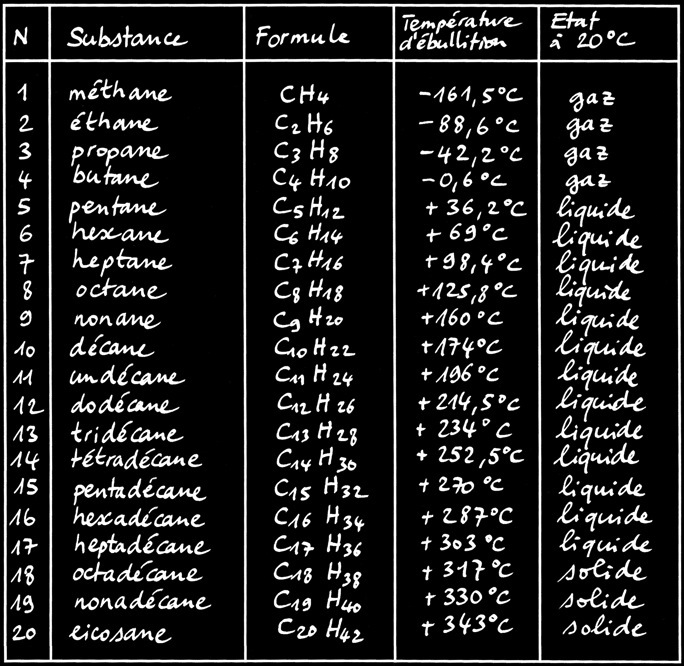
Le nom d’un alcane est déterminé par sa longueur. Il suffit de compter le nombre de carbone de la chaîne qui donne le début du nom: les préfixes «méth-, éth-, prop-, but-, pent-,...» et de rajouter le suffixe «ane» qui est la marque de tous les alcanes.
Nom
Tableau des 20 premiers alcanes linéaires (sans ramifications).

liaison σ
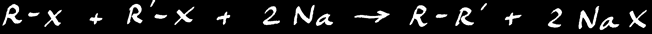






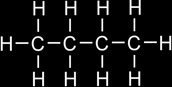
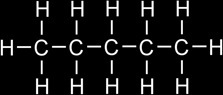
Comment s’appellent ces 2 alcanes?




Retrouve à l’aide du tableau ci-dessus le seul alcane liquide à température et pression ambiante. Clique dessus.








pétrole brut
essence
kérosène
diesel
mazout
distillat
paraffine
soufre
résidu