Moteur à combustion


Suite du cours: la combustion
Retour au portail des sciences



Retour au portail de chimie




Suite du cours: oxydation et réduction









Fin de la page
L'énergie produite lors d'une réaction de combustion dégage beaucoup de chaleur. On parle d'énergie calorifique (ou thermique): on dit que la réaction est exothermique. On peut utiliser cette chaleur de différentes façons pour créer du mouvement. La machine à vapeur a permis dès 1750 une grande révolution industrielle.

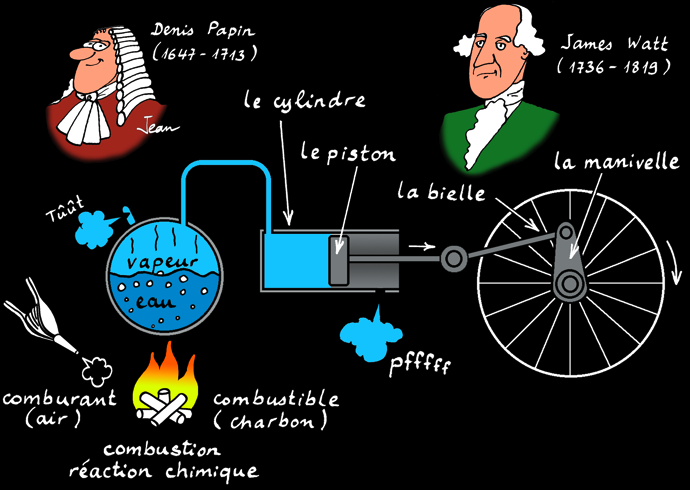
La machine à vapeur
La machine à vapeur est un moteur à combustion externe: la réaction a lieu à l'extérieur du cylindre. L'énergie thermique produite par la réaction de combustion est transmise à une chaudière qui contient de l'eau. Arrivée à la température d'ébullition, l'eau passe de l'état liquide à l'état gazeux (vapeur). Cette vapeur occupe un plus grand volume et exerce une pression dans la chaudière. La vapeur est canalisée dans un tuyau jusqu'à une chambre (le cylindre) dont une des parois est mobile: le piston). Le piston se déplace en coulissant dans le cylindre: on a transformé l'énergie thermique en énergie mécanique: un mouvement linéaire.
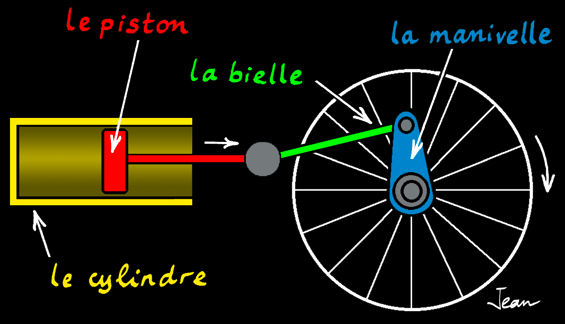
Le système bielle-manivelle est un système mécanique qui transforme un mouvement linéaire alternatif en un mouvement de rotation.
Avantage: on peut utiliser n'importe quel combustible (charbon, bois, pétrole ,..) et faire tourner des machines en absence de vent (moulin à vent) et loin des rivières (moulin à eau).
Inconvénient: il faut attendre que la chaudière produise de la vapeur et les pertes de chaleur sont énormes.
La machine à vapeur reçoit différents perfectionnements entre 1760 et 1790.

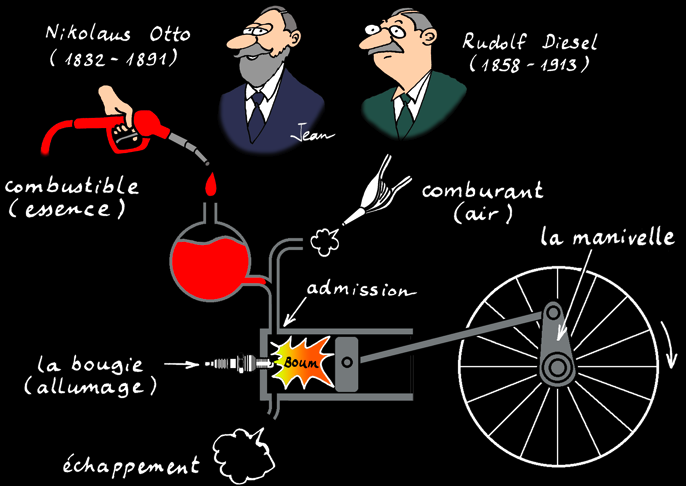
Le moteur à essence




Expérience





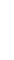


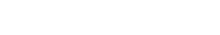

Le modèle réduit de l’entreprise allemande VILESCO permet de faire fonctionner une vraie machine à vapeur.
le sifflet
la chaudière
le tiroir
le cylindre
le piston
la bielle

La double action permet un gain de puissance. Le tiroir (en jaune) permet de faire passer alternativement la vapeur devant et derrière le piston. Il est commandé par le mouvement du piston lui-même: c’est un exemple génial de rétroaction.
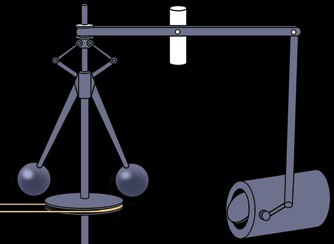
le régulateur à boules


Le projectile
Le moteur thermique ou moteur à «explosion» utilise un combustible liquide. C’est un moteur à combustion interne. La combustion à lieu directement dans le cylindre: il y a moins de pertes de chaleur que dans la machine à vapeur (moteur à combustion externe).

Le moteur à réaction
le réservoir


la combustion à lieu dans le cylindre
Un projectile (balle, boulet) est un véhicule un peu spécial. Il est destiné à ne faire qu’un voyage aller mais le principe est toujours le même: la réaction produit des gaz très chauds qui se dilatent et exercent une pression sur les parois. Celles de la douille (le cylindre) résistent tandis que la balle est projetée.
la combustion de la poudre à lieu dans un cylindre qu’on appelle la douille.
(douille en laiton)
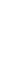
la balle est une sorte de piston sans retour.
(balle 9mm en cuivre)



conduite d’échappement de la vapeur
la roue :
mouvement rotatif

Locomotive «The Rocket» de Stephenson, 1829
Le régulateur à boules est un système qui permet de régler la vitesse de rotation de la machine à vapeur.
La réaction de combustion est exothermique (elle dégage de la chaleur): les gaz d’échappement se dilatent sous l’effet de cette chaleur et se projettent vers la sortie à l’arrière tout en repoussant par réaction la fusée vers l’avant.

On arrive à un résultat similaire sans réaction de combustion. L’échappement de l’air sous pression à l’arrière de la voiture (action) repousse par réaction le véhicule vers l’avant.

La flamme du chalumeau oxyhydrique
Mon chalumeau bricolé à partir d’un stylo à billes opère un mélange de gaz dihydrogène H2 et dioxygène O2. La réaction d’oxydation est très exothermique. On obtient une flamme de 2500°C. L’équation chimique s’écrit:









Système initial: les réactifs
Système final: les produits
Réaction
2 molécules de dihydrogène et
1 molécule de dioxygène
2 molécules de vapeur d’eau

Il faut mélanger les gaz dans un rapport stoechiométrique: 2 volumes de dihydrogène H2 pour 1 volume de dioxygène O2.

Locomotive Wolf, Magdeburg, 1860


