Réaction chimie organique

Nous allons d'abord étudier les réactions en chimie organique sous deux aspects :
La réaction homolytique est une réaction symétrique: le système final fait apparaître deux radicaux libres, sans charges, mais porteurs chacun de l'électron qu'il avait mis dans la liaison.
b)Réaction hétérolytique ( ou polaire )
Lors de la rupture de la liaison entre deux atomes, on peut envisager deux cas. Soit X et Y : deux atomes.
Pour les besoins de l'explication, la liaison X - Y sera représentée:
a)Réaction homolytique ( ou radicalaire )
Il s'agit d'un processus dissymétrique laissant apparaître des ions. Ce type de réaction n'est possible que dans un liquide polaire, favorisant ainsi la formation d'ions (voir les électrolytes).
Nous pouvons classer en chimie organique les réactifs en deux catégories:


rupture homolytique
rupture hétérolytique


Aspect électronique des réactions

Aspect énergétique et cinétique des réactions
a)Réaction élémentaire :


Fin de la page
Suite du cours: Classification des réactions
Retour au portail des sciences

Retour au portail de chimie


1.
2.
l'aspect énergétique et cinétique des réactions.
l'aspect électronique des réactions.
1.
2.
une réaction passe par le plus stable des intermédiaires possibles .
un catalyseur abaisse l'énergie d'activation .
b)Réaction complexe :
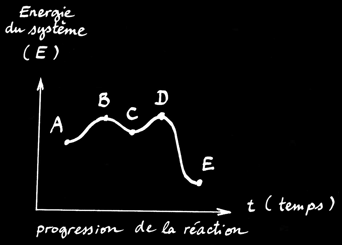

Remarques:
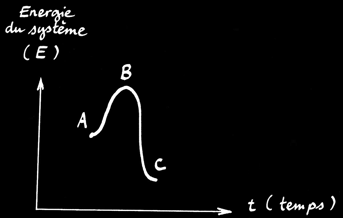
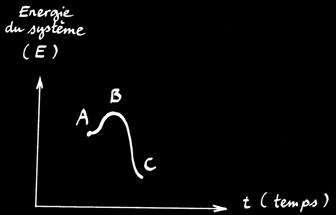


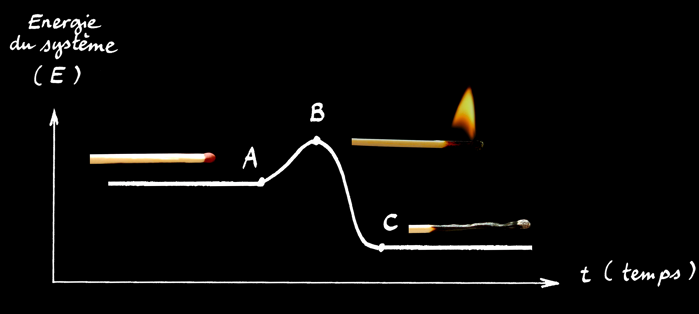


On définit l’énergie d’activation ( EA ) comme l’énergie qu’il faut fournir au système pour qu’il puisse passer de l’état A à l’état B. Dans le cas de l’allumette elle est fournie par le frottement sur la boîte.
EA
ER

On définit l’énergie de réaction ( ER ) comme la différence d’énergie entre l’état initial A et l’état final C du système.
Remarque:
S’il n’y avait pas d’énergie d’activation, le système évoluerait spontanément de l’état initial vers l’état final ... l’allumette s’allumerait “toute seule” dans sa boîte.
toute la chimie des réactions hétérolytiques (les plus nombreuses) est commandée par cette dualité électrophile-nucléophile .
Remarque:





porteurs d'une orbitale vide (cations), ils sont donc amateurs d'électrons (oxydants) et ont un caractère acide.
porteurs d'un doublet libre ( anions ), ils sont amateurs de noyaux positifs (réducteurs) et ont un caractère basique.
Réactifs électrophiles:
Réactifs nucléophiles:


