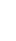Extraction du sel d’une roche salée










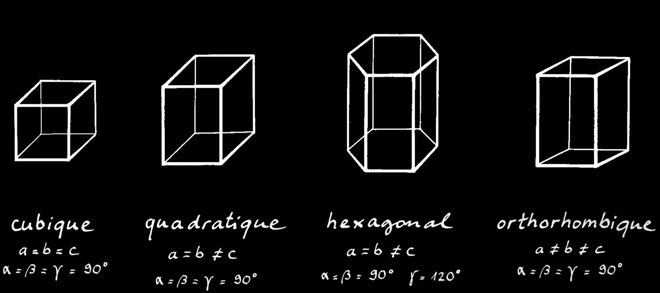
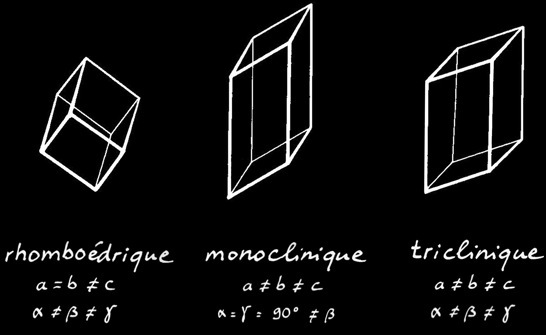
Les 7 systèmes cristallins
Nous avons récolté ......... g de sel.
La roche a une teneur en sel de .......... %.
Nous savons quelles transformations le sel a subies avant de parvenir sur notre table.
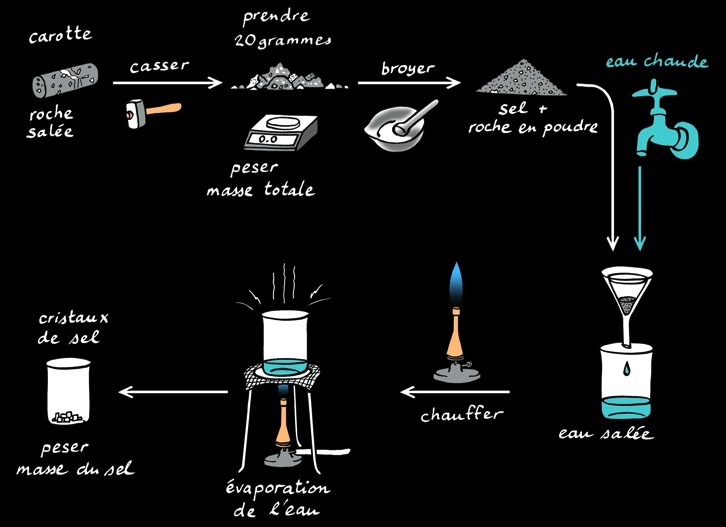
Dans les mines de Bex, on exploite une roche salée formée il y a 200 millions d'années dans une mer qui occupait la place des Alpes. La roche salée (brèche salifère des mines de Bex) est un mélange hétérogène. Le sel peut être séparé du reste de la roche grâce à une extraction à l'eau chaude. On se fonde ainsi sur une propriété qu'a le sel de se dissoudre dans l'eau alors que le reste de la roche est insoluble. Il reste à filtrer l'eau salée et récupérer le sel après évaporation de l'eau.
Buts de l'expérience
1 bec Bunsen
1 filtre
1 allume-gaz
1 marteau
1 pilon
1 mortier
1 entonnoir
1 trépied
1 noix double
1 becher 400 ml
1 petite pince
de l'eau chaude
1 anneau
1 balance
1 carotte de roche salée
Croûte de sel, Lac Natron (Tanzanie)
Cristaux de sel,
Mer Morte (Israël)
Carotte de roc salé, Mines de Bex (Suisse)
Sel de cuisine, issu des Mines de Bex (Suisse)
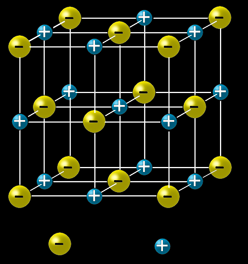
Une goutte d’eau salée. L’eau s’est évaporée: restent les cristaux cubiques de halite (NaCl). Grossi 10x
Comme beaucoup de substances utilisées par l'homme, le sel se trouve très rarement naturellement pur. On peut l'extraire directement de l'eau de mer dans les marais salants.
Montagne de sel et marais salants aux Salins de Giraud, Camargue (France)
Le sel récolté est bien pur. Il est blanc et son goût est caractéristique.



Roche (gris clair, opaque)
Veine de sel (gris foncé, vitreux)
Le sel n’est pas dispersé uniformément dans la roche:
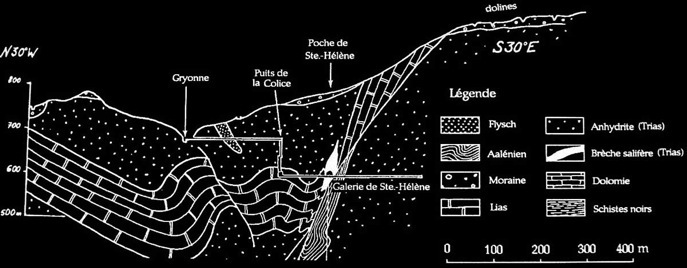
Coupe à travers une galerie des salines de Bex (d’après H. Badoux, 1966)
Réduire la roche en poudre avec un marteau puis le pilon et le mortier.
Peser l’échantillon de roche.
Préparer le papier filtre (pliage).
1.
2.
3.
Lors de l'ébullition, l'eau salée gicle hors du becher contrairement à l'eau pure: il faut placer au-dessus du becher un entonnoir à l'envers ou une grille afin de recueillir le sel projeté à l'extérieur.
Si la roche n'est pas parfaitement broyée, il reste du sel emprisonné à l'intérieur des petits grains: la teneur en sel que nous avons calculée (%) est donc sous-estimée.
En observant à la loupe binoculaire des grains de sel de cuisine (qui proviennent pour le Canton de Vaud des salines de Bex), on remarque qu'il s'agit de cristaux qui ont pour la plupart la forme de petits cubes.
En comparant nos résultats avec les autres groupes, nous remarquons que les valeurs sont très différentes. Les causes sont multiples: maladresse de certains expérimentateurs mais surtout hétérogénéité de la roche salée (l'échantillon est non représentatif car trop petit).
1.
2.
3.
4.
Le sel de cuisine ou chlorure de sodium (NaCl) a une grande importance non seulement dans l'alimentation, mais aussi dans toutes sortes d'activités industrielles: fabrication de la soude, du savon, tannage des peaux ou conservation des aliments. Il fut même utilisé comme monnaie d'échange: le salaire.
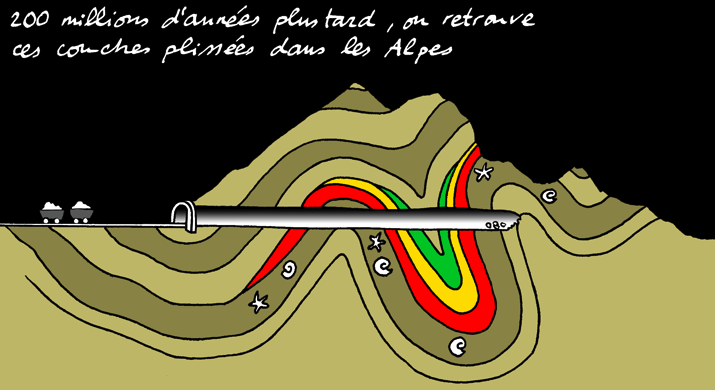
Le chlorure de sodium prend le nom de halite (ou sel gemme) lorsqu'il se trouve sous forme de cristaux. Ceux-ci ont la forme de cubes: on dit que le NaCl cristallise dans le système cubique.
Extraire le sel de la roche.
Calculer la teneur en sel (%) de cette roche.
1.
2.
Matériel
Teneur en sel de la roche de Bex:
Le sel de cuisine (chlorure de sodium) est additionné de fluorure (prévention de la carie dentaire) et de iodure (prévention contre le goître). Son utilisation généralisée permet de toucher toute la population.
L’antiagglomérant E536 est le ferrocyanure de potassium K4[Fe(CN)6]. Il empêche les grains de sel de se coller les uns aux autres dans une atmosphère humide. Il est aussi utilisé en oenologie pour éliminer les traces de métaux dans le vin.

4.
5.
6.
7.
8.
9.
Verser la poudre obtenue dans l’entonnoir (filtre).
Rajouter de l’eau bouillante (elle dissout mieux le sel que l’eau froide).
Laisser égoutter l’eau salée dans le becher.
Rajouter de l’eau chaude pour laver la boue de roche restée dans le filtre.
Faire bouillir l’eau salée recueillie afin d’évaporer toute l’eau: le sel se cristallise au fond.
Récolter le sel et peser.

1.
2.
3.
4.
H. Badoux. Mines de sel de Bex, aperçu géologique et minier. Aminsel, Bex, 1982.
-
G.D. de Segonzac. Les chemins du sel. Découvertes Gallimard, Paris, 1991.
-
H.Badoux, H.-H. Gabus. Feuille 1285 Les Diablerets. Atlas géologique de la Suisse, Service hydrologique et géologique national, 2e ed, 1991.
Visite des mines de Bex: http://www.mines.ch


sodium Na+
chlorure Cl-
5.
6.





5.
Wikipedia, Le sel alimentaire http://fr.wikipedia.org/wiki/Sel_alimentaire


Introduction

Méthode

Résultats

Remarques

Conclusions

Références
1.
2.
3.



masse du sel / masse de la roche X 100 =........................ %


Fin de la page

Formation du sel des Alpes
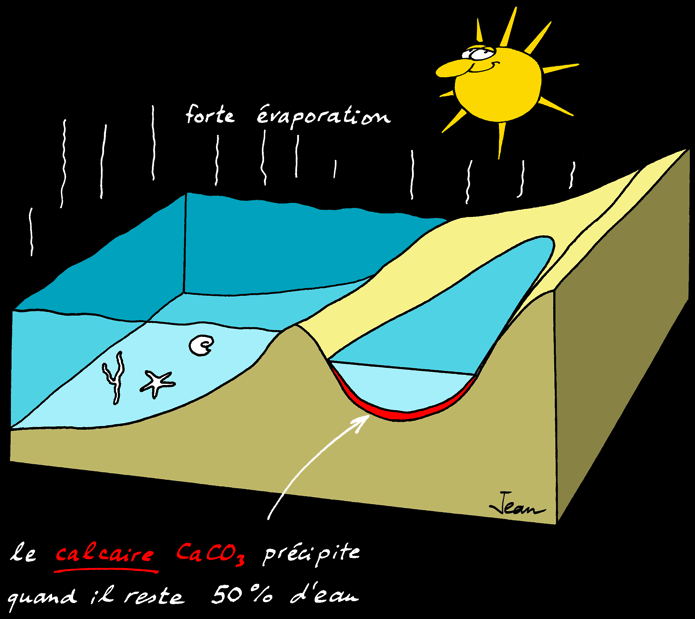
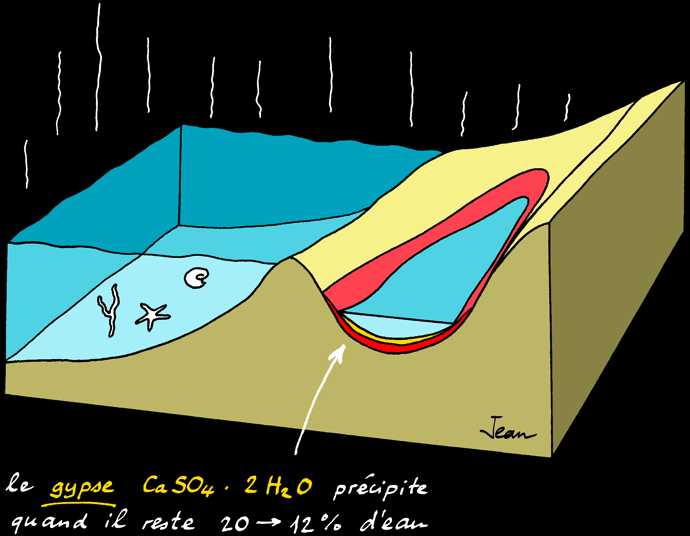
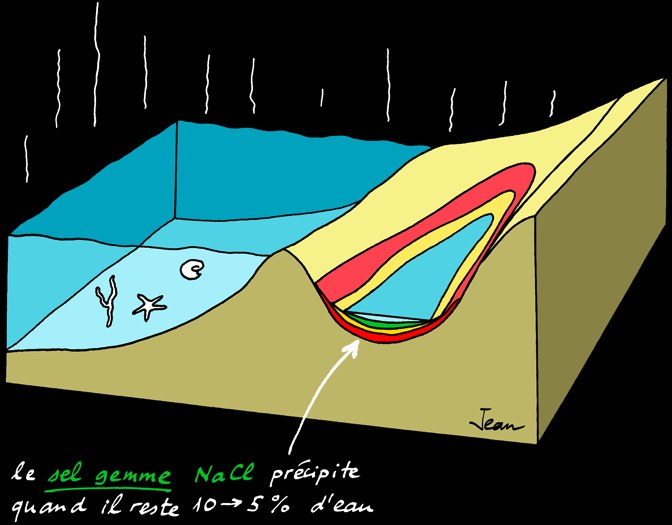
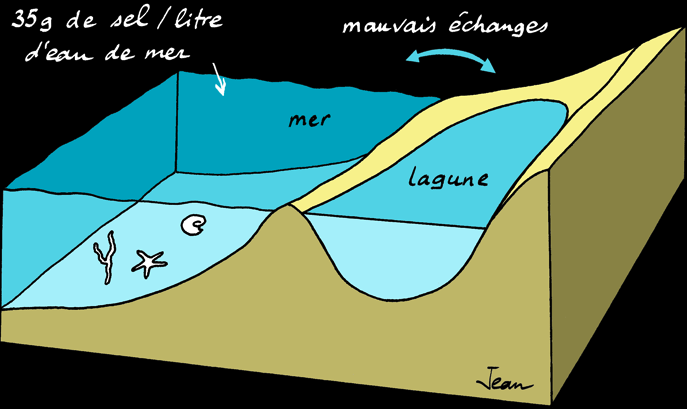
Au delà d'une certaine limite, les sels ne sont plus solubles et précipitent (ils tombent au fond) les uns après les autres. L'ordre dans lequel les sels précipitent s'appelle séquence évaporitique :
% d'évaporation
d'eau de mer
50 %
80 %
90 %
95 %
Dans un marais salant, on utilise le soleil et le vent pour extraire le sel de cuisine (ou halite, NaCl). Les pluies ralentissent la production.
La salinité des océans est en moyenne de 35 g/l. Elle varie entre 30 g/l (Atlantique nord) et 40 g/l (mer Rouge). La mer Morte a une salinité supérieure (330 g/l) car c'est une mer fermée.
Anions
Chlorure
Sulfate
Hydrogénocarbonate
Bromure
Carbonate
Fluorure
Hydroxyde
Cations
Sodium
Magnésium
Calcium
Potassium
Les évaporites ou roches évaporitiques sont des roches sédimentaires salines. L'eau de mer contient environ 35 grammes de sels dissous par litre (35 g/l ou 3,5% de la masse). Lorsque l'eau s'évapore, il reste une saumure de plus en plus concentrée.
Sels
Calcite
Dolomite
Gypse
Halite
Sels de magnésium
Sels de potassium
Formule chimique
CaCO3
CaMg(CO3)2
CaSO4
NaCl
MgSO4
KCl
g/kg
19,3524
2,7123
0,1080
0,0673
0,0156
0,0013
0,0002
10,7837
1,2837
0,4121
0,3991
Formule
Cl-
SO4--
HCO3-
Br-
CO3--
F-
HO-
Na+
Mg2+
Ca2+
K+
mol/kg
0,54586
0,02824
0,00177
0,00084
0,00026
0,00007
0,00001
0,46907
0,05282
0,01028
0,01021
Composition moyenne de l’eau de mer

Retour au portail de physique

Retour au portail des sciences



Retour au portail de géologie



Retour au portail de chimie







Visiter les roches sédimentaires



cristal cubique de halite